
来源:财经报道网
2026-05-05 21:31:58
(原标题:香雪制药国内TCR-T细胞治疗抗癌新药确证性临床试验正式启动)
近日,香雪生命科学技术(广东)有限公司(简称“香雪生命科学”或“XLifeSc”)针对中国首个TCR-T细胞治疗产品TAEST16001注射液开展的治疗肿瘤抗原NY-ESO-1表达阳性、基因型为HLA-A*02:01的晚期软组织肉瘤的多中心、开放、单臂确证性临床试验召开了项目启动会。TAEST16001注射液是中国首个获批IND、被CDE纳入突破性治疗品种且首个进入确证性临床试验的TCR-T细胞治疗产品。本次临床试验启动会的召开,标志着我国在实体瘤细胞治疗领域迈出了重要一步!该产品有望成为中国第一款上市的TCR-T细胞治疗药物,对中国免疫细胞治疗创新药的发展具有里程碑意义。

该临床试验的申办方是香雪生命科学,两家临床中心分别是中山大学肿瘤防治中心(以下简称“中肿”)与北京大学肿瘤医院(以下简称“北肿”)。香雪生命科学分别与两家临床中心于4月17日、4月30日在北京、广州召开了项目启动会。会上,主要研究者(PI )与相关专家及各方负责人围绕本项目的研究设计、研究方案(入选标准、排除标准等)及风险管控等方面展开了充分讨论并达成共识,为后续项目的开展做好了充分准备。
中肿PI张星教授表示:“基于前期TAEST16001注射液在晚期肉瘤探索中取得的积极结果,我们对本次确证性临床研究的顺利推进充满信心。该研究有望进一步验证靶向NY-ESO-1的TCR-T疗法的临床价值,为热切渴望新的治疗选择的晚期肉瘤患者带来希望。我们期待在多方协作下,研究高质量完成,早日为更多患者带来福音。”
北肿PI樊征夫教授表示:“TAEST16001注射液在前期临床试验中展现出了良好的疗效和安全性,受到国内外同行广泛关注,同时也受到众多患者的热切期盼。我们对此次确证性临床试验充满信心,同时也将严格按照试验方案,确保试验数据的科学性和可靠性,为产品的上市提供有力的支持。”
香雪生命科学CEO曾仑表示:“TAEST16001注射液继获得CDE纳入突破性疗法药品后,成为中国首个获批开展确证性临床试验的TCR-T细胞治疗产品,标志着我国在实体瘤细胞治疗领域迈出了重要的一步。这不仅是香雪生命科学的里程碑,更是中国免疫细胞治疗创新药发展的重要突破。感谢北京大学肿瘤医院和中山大学肿瘤防治中心作为组长单位,感谢张星教授、樊征夫教授以及所有参与前期临床试验的研究者们。正是你们严谨的科学态度和卓越的临床研究能力,让TAEST16001注射液在I期和探索性II期临床试验中显示了良好的临床疗效,为治疗晚期实体瘤带来了新的希望。这次确证性临床试验的启动,意味着我们距离让这款创新药惠及更多患者又近了一步。我们期待TAEST16001注射液能够加快推进成为中国第一款上市的TCR-T细胞治疗药物,冲击成为全球第二款治疗实体瘤的TCR-T细胞治疗产品。”
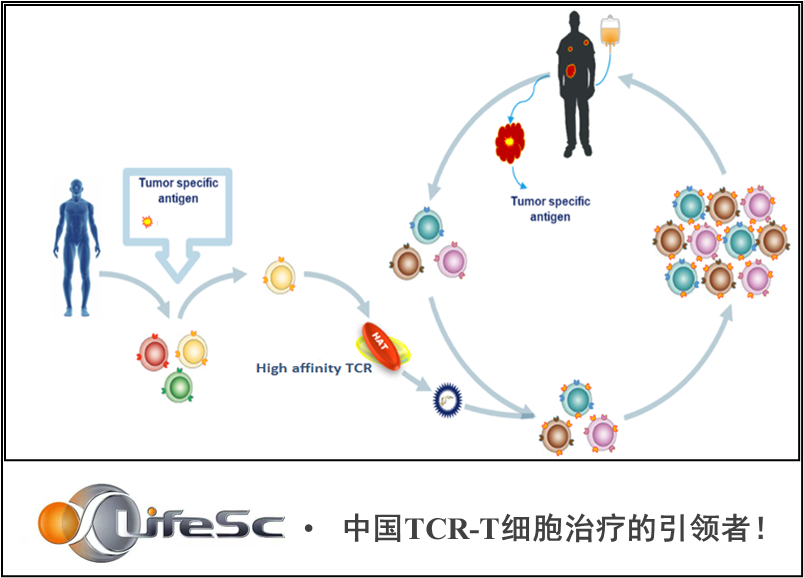
TCR-T疗法是一种过继免疫细胞治疗(Adoptive Cell Transfer Therapy,ACT),是指从肿瘤患者体内分离免疫活性细胞,在体外进行工程化改造与扩增,然后向患者回输,从而达到直接杀伤肿瘤或激发机体的免疫应答杀伤肿瘤细胞的目的。本研究中的TAEST16001注射液是由香雪生命科学自主研发,针对NY-ESO-1癌睾抗原的TCR-T细胞: 先通过携带肿瘤抗原特异性TCR基因的慢病毒载体,在体外对患者的T细胞进行基因工程改造,再将这些T细胞扩增至1×109~2×1010个的细胞量,患者经过适当剂量的淋巴细胞清除预处理后,回输TCR-T细胞。在I期、II临床试验中,TAEST16001注射液的安全性和有效性均得到了验证。经与CDE沟通讨论后,获准开展此项可作为支持本品用于治疗软组织肉瘤适应症申请附条件上市的关键确证性临床试验。
【关于香雪生命科学】
香雪生命科学技术(广东)有限公司(简称“香雪生命科学”或“XLifeSc”)是香雪制药控股子公司,是一家聚焦TCR领域的细胞免疫治疗产品和技术的研发企业,是国内TCR-T细胞免疫治疗的头部企业。公司以“解决人类健康难点,树立肿瘤治疗标杆”为愿景,以“聚焦TCR,赋能T细胞,攻克实体瘤”为使命。
香雪生命科学具有自主知识产权的TCR核心技术,拥有完整的TCR-T细胞治疗产品研发平台和生产制备体系,其中TCR-T细胞治疗产品研发平台包含:①抗原肽发现平台,②TCR亲和力优化平台,③高通量TCR-T安全性筛查平台;TCR-T细胞治疗产品生产制备体系包含:①自动化细胞生产平台,②质控平台。已形成TCR-T细胞产品全链条的创新产业链。
香雪生命科学TCR-T产品和储备管线布局广泛,靶点丰富涉及包括CT抗原、新生抗原和病毒抗原等几乎所有与肿瘤相关的特异性抗原,涵盖A0201、A1101及A2402等多个以中国人群居多的HLA基因型,适应症覆盖多种临床难治的实体瘤,处于国际领先水平。
目前,香雪生命科学有三个产品已在中国获得IND批件,其中第一个产品是TAEST16001,适应症为软组织肉瘤(后拓展食管癌和非小细胞肺癌),目前在中国完成I期临床试验和II期临床试验第一阶段的研究工作,被纳入突破性治疗品种名单,进入确证性临床试验阶段,有望成为中国第一个全球第二个上市的TCR-T细胞治疗产品;第二个产品是TAEST1901,适应症为肝癌、胃癌,正在启动I期临床试验;第三款产品是XLS-103,靶向KRAS G12V/HLA-A*11:01,适应症为晚期胰腺癌、非小细胞肺癌,目前已分别获批IND,正在筹备I期临床试验。
本文来源:财经报道网
证券之星网站
2026-05-06
财经报道网
2026-05-06
财经报道网
2026-05-06
财经报道网
2026-05-06
财经报道网
2026-05-06
财经报道网
2026-05-05
证券之星资讯
2026-05-06
证券之星资讯
2026-05-06
证券之星资讯
2026-05-04

